HPLC和LC/MS 緩沖液選擇指南:為什么要控制PH值?
適用于HPLC和LC/MS的緩沖液
如果樣品中含有離子化化合物,對于反相HPLC(RP-HPLC)分離,流動相pH值可作為控制保留的最重要的變量之一。
然而,如果控制不當,pH值也可能誘發諸多問題。
由于經RP-HPLC分析的大多數化合物含有一個或多個酸性或堿性官能團,因此大多數流動相需要控制pH值。
基于此,緩沖液的使用非常廣泛。本手冊為實際操作的色譜分析人員重點介紹了流動相pH值的一些重要方面。
為什么要控制PH值?
圖1表明,如果存在離子化化合物,則需要控制pH值。
如果酸性溶劑pKa上下浮動超過2個pH單位,則至少99%的部分將分別離子化或非離子化。
低于其pKa時,堿基將被離子化;而超過其pKa時,將被非離子化。
非離子化形式將具有較小的極性(更疏水),因此在反相體系中能夠更加有效地保留下來。
所以,pH值較低時,會保留更多的酸性(圖1a),而在高pH值下,會保留更多的堿性(圖1b)。
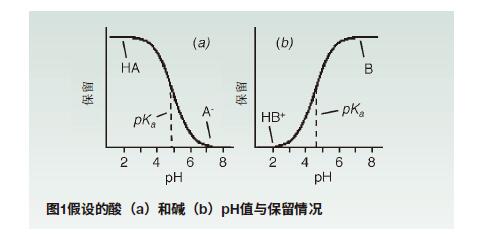
圖2a說明了部分化合物對pH的微小變化極為敏感。0.1個pH單位的變化就會導致分辨率兩倍的變化,這是許多實驗室常見的pH調節誤差量。
圖2b顯示了酸性、堿性和中性化合物pH值與保留情況的關系。
pH為3時,其保留情況比pH為5時更加敏感(對于酸性),而對于堿性,則pH需要大于等于6。而且,當pH接近pKa時,保留時間將不穩定;如果存在類似結構的化合物,相應的峰值間距(選擇性)會發生改變。

圖2 流動相pH值的微小變化對分離的影響。
(a)堿性分析物:對氨基苯甲醚、間甲苯胺、對氯苯胺、間氨基苯甲腈(按保留次序);27:73甲醇/磷酸鹽緩沖液。
(b)酸性(酸):水楊酸;堿;甲基苯丙胺;中性;非那西丁。
在選擇流動相pH時還應考慮的另一個因素是色譜柱的穩定性。
一般來說,硅基色譜柱應在2<pH<8的條件下操作。在pH<2時,由于可能發生水解而導致鍵合相的損失。
pH大于8時,硅膠骨架可溶性變強。較高純度的硅膠比較低純度的產品更耐受較高的pH值。
另一個較為復雜的問題是,硅膠顆粒表面上可能會電離出未鍵合的硅醇(-Si-OH)基團。
對于較老的、純度低的硅膠(通常稱為“A型”硅膠),這些硅醇基團的pKa在pH4-5的范圍內。也就是說,在pH>6時,這些材料會發生顯著的硅烷醇電離。
為什么要控制PH值?
一直以來這都是通過陽離子交換過程使堿性化合物達到峰拖尾的主要原因。
較新的高純度(“B型”)硅膠的pKa>7,因此由離子化硅烷醇位點的陽離子交換引起的峰拖尾是最小的。
因此,高純度硅膠比較老的硅膠的峰形更好,正如圖3所示分離中的幾種堿基成分那樣。
除了峰形得到改善之外,由于這些不可預測的次級硅烷醇相互作用的減少,高純度硅膠比低純度硅膠具有更好的再現性。
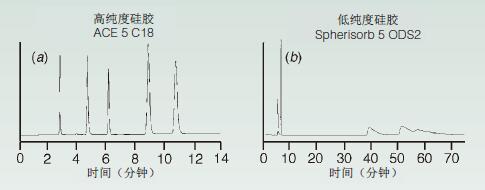
圖3. 高純度硅膠在減少堿基硅烷醇拖尾的效果。
成分:去甲麻黃堿、去甲替林、甲苯(中性)、丙咪嗪、阿米替林。
條件:250 x 4.6 mm, 5μm
色譜柱;80:20甲醇/25 mM 磷酸鹽(pH 6.0);1.00mL/min
為什么要控制PH值?未完.....待續



